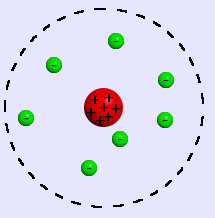
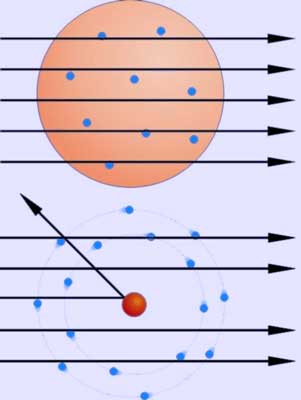
Το ατομικό μοντέλο του Rutherford περιέχει δύο βασικά μειονεκτήματα:
(α) Δεν εξηγεί τη σταθερότητα του ατόμου
Ξέρουμε πως τα ηλεκτρικά φορτία εκπέμπουν ηλεκτρομαγνητική ακτινοβολία και έτσι χάνουν ενέργεια. Έτσι, τα ηλεκτρόνια ενός ατόμου, κατά την περιφορά τους γύρω από τον πυρήνα (επειδή επιταχύνονται) θα έπρεπε να εκπέμπουν ηλεκτρομαγνητική ακτινοβολία. Η απώλεια όμως της ενέργειας θα ελάττωνε την ακτίνα της τροχιάς του ηλεκτρονίου και έτσι τα ηλεκτρόνια θα εκτελούσαν σπειροειδή τροχιά γύρω από τον πυρήνα μέχρι τελικά να συγκρουστούν με αυτόν. Αυτό όμως δεν συμβαίνει στην πραγματικότητα γιατί το άτομο είναι σταθερό.
(β) Δεν εξηγεί το γραμμικό φάσμα εκπομπής τω αερίων (κυρίως του υδρογόνου)
Με την εκπομπή της ενέργειας, η ακτίνα της τροχιάς των ηλεκτρονίων θα έπρεπε να μικραίνει και η συχνότητα περιφοράς τους γύρω από τον πυρήνα να παίρνει διαδοχικές τιμές. Όπως ξέρουμε, η συχνότητα των εκπεμπόμενων ηλεκτρομαγνητικών κυμάτων θα έπρεπε να είναι ίση με τη συχνότητα περιφοράς του ηλεκτρονίου. Καθώς τα ηλεκτρόνια θα ακτινοβολούσαν συνέχεια, οι γωνιακές τους ταχύτητες θα μεταβάλλονταν κατά συνεχή τρόπο και θα εξέπεμπαν ένα συνεχές φάσμα και όχι το γραμμικό φάσμα που παρατηρείται στην πράξη.
1) E. Rutherford, The Scattering of α and β Particles by Matter and the Structure of the Atom, Phil. Mag. 6, vol. 21, 669-688 (1911). Rutherfords Artikel im Philosophical Magazine
Από τη ελληνική Βικιπαίδεια http://el.wikipedia.org . Όλα τα κείμενα είναι διαθέσιμα υπό την GNU Free Documentation License